高中化学知识点:溶液质量分数的计算
逍遥右脑 2017-04-23 10:35
溶液质量分数的计算:
(1)溶质的质量分数=
(2)溶质的质量分数、溶质的物质的量浓度及溶液密度之间的关系:
①溶质的质量分数=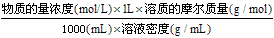
②物质的量浓度=
版权声明:本文内容由互联网用户自发贡献,该文观点仅代表作者本人。本站仅提供信息存储空间服务,不拥有所有权,不承担相关法律责任。如发现本站有涉嫌抄袭侵权/违法违规的内容,请发送邮件至 lxy@jiyifa.cn 举报,一经查实,本站将立刻删除。
(1)溶质的质量分数=

(2)溶质的质量分数、溶质的物质的量浓度及溶液密度之间的关系:
①溶质的质量分数=
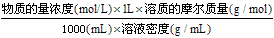
②物质的量浓度=

有关溶液密度的问题:
1.溶液质量分数与密度的关系
(1) 越大,则ρ(溶液)越大,常见溶液如NaCl溶液、硫酸溶液等。
越大,则ρ(溶液)越大,常见溶液如NaCl溶液、硫酸溶液等。
(2) 越大,则ρ(溶液)越小,常见溶液如氨水、酒精溶液等。
越大,则ρ(溶液)越小,常见溶液如氨水、酒精溶液等。
2.溶液混合后质量分数的变化规律
质量分数分别为 的两溶液(同种溶质)混合,混合后溶液的质量分数为ω。
的两溶液(同种溶质)混合,混合后溶液的质量分数为ω。
(1)等体积混合
若是加等体积水稀释,可视 中其一为0 分析。
中其一为0 分析。
(2)等质量混合:
版权声明:本文内容由互联网用户自发贡献,该文观点仅代表作者本人。本站仅提供信息存储空间服务,不拥有所有权,不承担相关法律责任。如发现本站有涉嫌抄袭侵权/违法违规的内容,请发送邮件至 lxy@jiyifa.cn 举报,一经查实,本站将立刻删除。