初中化学知识点:催化剂和催化作用
逍遥右脑 2015-12-22 10:11
催化剂及催化作用的概念:
催化剂的特点:
催化剂概念的要点可概括为“一变”“二不变”。
(1)“一变”是指催化剂能改变其他物质的化学反应速率,这里“改变”包括加快和减慢,也就是说催化剂可以加快反应速率,也可以减慢反应速率。
(2)“二不变”指催化剂本身的化学性质不变。
易错点:
①催化剂一般有选择性,即仅能对某一反应或某一类型的反应起催化作用。如二氧化锰是过氧化氢分解的催化剂,但对其他的反应不一定是。
②对某些反应来说,催化剂也可能不止一种,如能催化过氧化氢分解的催化剂除二氧化锰外,还有硫酸铜溶液、红砖粉(主要成分为氧化铁)等。
③催化剂可以重复使用。
催化剂在化工生产中的作用:
催化剂在化工生产中有重要作用,人多数化工生产都有催化剂参与。例如,在石油炼制过程中,用高效催化剂生产汽油、煤油等;在汽车尾气处理,归用催化剂促进有害气体的转化;酿造工业和制药工业都要用酶作催化剂,某些酶制剂还是宝贵的药物。
相关初中化学知识点:化合价的写法和意义
化合价的定义:
一种元素一定数目的原子跟其他元素一定数目的原子相化合的性质,叫做这种元素的化合价。化合价有正价、负价之分,如在H2O中,氢原子与氧原子的个数比为2:1,H为+1价,0为-2价;在MgCl2中,镁原子与氯原子的个数比为1:2,Mg为+2价,Cl为-1价。
化合价的意义:
化合价反映元素的原子之间相互化合时的数日,是元素的一种性质。因此,强调化合价时,一定要指明元素。
化合价的表示方法:
通常在元素符一号或原子团的正上方用+n或-n表示,“+”“-”在前,数值在后。“1”不能省略。例如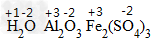 .
.
化合价的一般规律:
(1)化合价有正价和负价;
(2)金属元素跟非金属元素化合时,金属元素显正价,非金属元素显负价,如MgCl2中Mg为+2价,Cl为-1价;非金属元素和氧元素形成化合物时,非金属元素通常显正价,氧元素通常显-2价,如SO2中S为+4价,O为-2价;
(3)一些元素在不同物质中可显不同的化合价,如KMnO4、K2MnO4中锰元素的化合价分别为+7,+6价;
(4)化合物中,各元素正、负化合价代数和为0;
(5)因为化合价是元素的原子在形成化合物时才表现出来的一种性质,所以单质中元素的化合价为0;
(6)原子团不能独立存在,只是化合物的一个组成部分,所以原子团的化合价由各元素的正、负化合价的代数和算出,原子团的化合价一定不为0。
化合价与最外层电子数的关系:
(1)金属元素的化合价数值一般等于它的最外层电子数。
(2)非金属元素的最高正价数值等于它的最外层电子数(O、F除外),最低负价数值等于8减去最外层电子数。
化合价符号与离子符号的比较
一些常见元素和根的化合价:
记忆口诀:
常见元素的化合价口诀
(1)一价钾、钠、银、氢、氟,二价钙、镁、钡和锌,铝价正三氧负二,以上价态要记真。铜一二来铁二三,碳硅二四要记全,硫显负二正四六,负三正五氮和磷,氯价最常显负一,还有正价一五七,锰显正价二四六,最高价数也是七。
(2)常见原子团的化合价口诀
一价铵根氢氧根,另有硝酸氯酸根。二价硫酸碳酸根,勿忘一个锰酸根。三价只有磷酸根。除了铵根皆为负,常写常用能记住。
相关初中化学知识点:元素的推断
元素推断题:
元素推断题是中学化学练习中的一种重要题型,该类题型以原子结构、周期表等为题干,集基本概念、基础理论及元素化合物知识于一身,具有综合性比较强的特点。
元素推断的规律:
一、原子结构与元素在周期表中的位置关系的规律
1.周期数=核外电子层数
2.族序数=主族元素的最外层电子数
3.质子数=原子序数=原子的核外电子数
4.主族元素的最高正价=族序数
5.最低负价=最高正价-8
二、根据族序数与周期序数的比值判断金属性与非金属性的强弱(族序数―m;周期―n)
1.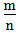 <1时,为金属,
<1时,为金属,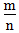 越小,金属性越强
越小,金属性越强
2.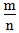 >1时,为非金属,
>1时,为非金属,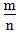 越大,非金属性越强
越大,非金属性越强
3.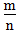 =1时,为两性元素
=1时,为两性元素
三、根据元素的性质,存在及用途的特殊性来推断元素
1.形成化合物种类最多的元素或单质是自然界中硬度最大的物质的元素,或气态氢化物中氢的质量分数最大的元素:C
2.空气中含量最多的元素或气态氢化物的水溶液呈碱性的元素:N
3.地壳中含量最多的元素,或气态氢化物沸点最高的元素,或氢化物在通常情况下呈液态的元素:O
4.地壳中含量最多的金属元素:Al
5.最活泼的非金属元素,或无正价的元素,或无含氧酸的非金属元素,或无氧酸可腐蚀玻璃的元素,或气态氢化物最稳定的元素,或阴离子的还原性最弱的元素:F
6.最活泼的金属元素,或最高正价氧化物对应的水化物碱性最强的元素,或阳离子氧化性最弱的元素:Cs
7.最容易着火的非金属元素的单质,其元素是:P
8.焰色反应:黄色:Na;紫色:K
9.最轻的单质的元素:H;最轻的金属元素:Li
10.常温下单质呈液态的非金属元素:Br;金属元素:Hg
11.两性元素:Al,Be,Zn
12.元素的气态氢化物和它的最高价氧化物对应的水化物起化合反应的元素:N
13.元素的气态氢化物能和它的氧化物在常温下反应,生成改元素的单质元素:S 14.常见的能形成同素异形体的元素:C,P,O,S
四、周期表中特殊位置的元素
1.族序数=周期数的元素:H,Be,Al
2.族序数=周期数2倍的元素:C
3.族序数=周期数3倍的元素:O
4.周期数是族序数2倍的元素:Li
5.周期数是族序数3倍的饿元素:Na
6.最高正价与最低负价代数和为零的短周期元素:C,Si
7.最高正价是最低负价绝对值3倍的短周期元素:S
8.除H外,原子半径最小的元素:F
9.短周期中离子半径最大的元素:S
10.最高正化合价不等于族序数的元素:F,O 五、元素周期表中的规律
五、元素周期表中的规律
1.各周期的元素种数(n表示周期序数)
(1)n为奇数: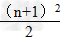
(2)n为偶数: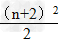
2.元素位置的确定
(1)根据原子结构示意图
①电子层数=周期序数
②最外层电子数=主族序数
(2)根据相近的稀有气体元素的原子序数:未知元素的原子序数-与之最接近的稀有气体元素的原子序数
①得数为正:该稀有气体的下一周期
②得数为负:与该稀有气体在同一周期
3.IIA族与IIIA族原子序数差值规律
(1)不跨过渡+1
(2)跨过过渡+11
(3)跨过锕镧+25
4.同主族元素的原子序数差值规律:左上右下规律
(1)IA族和IIA族(左):b=a+m
(2)IIIA族~VIIA族(右):b=a+n
(a:上一周期元素的原子序数;b:下一周期元素的原子序数;m:上一周期的元素种数;n:下一周期的元素种数)
5.阴上阳下规律:
(1)原子序数相同的阴阳离子,阴离子在上一周期,阳离子在下一周期
(2)离子半径:阴离子>阳离子
(3)原子半径:阴离子对应原子<阳离子对应原子
相关初中化学知识点:酸碱指示剂
酸碱指示剂:
跟酸或碱的溶液起作用而显示不同颜色的物质,叫酸碱指示剂,通常也简称指示剂。
紫色石蕊试液和无色酚酞试液的显色:
紫色石蕊试液和无色酚酞试液是两种常用的酸碱指示剂,它们与酸性、碱性溶液作用时显示的颜色见下表:
易错点:
①变色的是指示剂,而不是酸或碱的溶液。如盐酸使紫色石蕊试液变红,不能说成紫色石蕊试液使盐酸变红,但可以说紫色石蕊试液遇盐酸变红。
②酸或碱的溶液能使紫色石蕊试液或酚酞试液变色,但能使紫色石蕊试液或酚酞试液变色的不一定是酸或碱的溶液,还可能是酸性盐溶掖或碱性盐溶液。如碳酸钠溶液能使紫色石蕊试液变蓝,但碳酸钠不是碱,而是盐。
酸碱指示剂的代用品:
在自然界里,有许多植物色素在不同的酸碱性溶液中.都会发生特定的颜色变化。这些植物色素可以用作石蕊和酚酞等指示剂的代用品。一些植物的色素及其在酸碱性溶液中的颜色变化如下:
版权声明:本文内容由互联网用户自发贡献,该文观点仅代表作者本人。本站仅提供信息存储空间服务,不拥有所有权,不承担相关法律责任。如发现本站有涉嫌抄袭侵权/违法违规的内容,请发送邮件至 lxy@jiyifa.cn 举报,一经查实,本站将立刻删除。
| 概念 | |
| 催化剂 | 在化学反应中能改变其他物质的化学反应速率,而本身的质量和化学性质在化学反应前后都没有改变的物质。 |
| 催化作用 | 催化剂在化学反应中所起的作用 |
催化剂的特点:
催化剂概念的要点可概括为“一变”“二不变”。
(1)“一变”是指催化剂能改变其他物质的化学反应速率,这里“改变”包括加快和减慢,也就是说催化剂可以加快反应速率,也可以减慢反应速率。
(2)“二不变”指催化剂本身的化学性质不变。
易错点:
①催化剂一般有选择性,即仅能对某一反应或某一类型的反应起催化作用。如二氧化锰是过氧化氢分解的催化剂,但对其他的反应不一定是。
②对某些反应来说,催化剂也可能不止一种,如能催化过氧化氢分解的催化剂除二氧化锰外,还有硫酸铜溶液、红砖粉(主要成分为氧化铁)等。
③催化剂可以重复使用。
催化剂在化工生产中的作用:
催化剂在化工生产中有重要作用,人多数化工生产都有催化剂参与。例如,在石油炼制过程中,用高效催化剂生产汽油、煤油等;在汽车尾气处理,归用催化剂促进有害气体的转化;酿造工业和制药工业都要用酶作催化剂,某些酶制剂还是宝贵的药物。
相关初中化学知识点:化合价的写法和意义
化合价的定义:
一种元素一定数目的原子跟其他元素一定数目的原子相化合的性质,叫做这种元素的化合价。化合价有正价、负价之分,如在H2O中,氢原子与氧原子的个数比为2:1,H为+1价,0为-2价;在MgCl2中,镁原子与氯原子的个数比为1:2,Mg为+2价,Cl为-1价。
化合价的意义:
化合价反映元素的原子之间相互化合时的数日,是元素的一种性质。因此,强调化合价时,一定要指明元素。
化合价的表示方法:
通常在元素符一号或原子团的正上方用+n或-n表示,“+”“-”在前,数值在后。“1”不能省略。例如
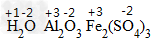 .
.化合价的一般规律:
(1)化合价有正价和负价;
(2)金属元素跟非金属元素化合时,金属元素显正价,非金属元素显负价,如MgCl2中Mg为+2价,Cl为-1价;非金属元素和氧元素形成化合物时,非金属元素通常显正价,氧元素通常显-2价,如SO2中S为+4价,O为-2价;
(3)一些元素在不同物质中可显不同的化合价,如KMnO4、K2MnO4中锰元素的化合价分别为+7,+6价;
(4)化合物中,各元素正、负化合价代数和为0;
(5)因为化合价是元素的原子在形成化合物时才表现出来的一种性质,所以单质中元素的化合价为0;
(6)原子团不能独立存在,只是化合物的一个组成部分,所以原子团的化合价由各元素的正、负化合价的代数和算出,原子团的化合价一定不为0。
化合价与最外层电子数的关系:
(1)金属元素的化合价数值一般等于它的最外层电子数。
(2)非金属元素的最高正价数值等于它的最外层电子数(O、F除外),最低负价数值等于8减去最外层电子数。
化合价符号与离子符号的比较
| 元素化合价的符号 | 离子符号 | |
| 概念不同 | 表示元素原子所显化合价的数值和正负的符号 | 表示带电原子(或原子团)所带电荷的电性核电荷量的符号 |
| 位置不同 | 化合价写在元素符号或原子团的正上方 | 所带电荷写在元素符合(或原子团)的右上角。 |
| 前后不同 | 正负号在前,数字在后 | 数字在前,正负号在后 |
| 省略不同 | 化合价为+1或-1价时,数字1不能省略 | 带一个单位正电荷或负电荷时,“1”不能省略不写 |
一些常见元素和根的化合价:
| 元素和根的名称 | 元素和根的符号 | 常见的化合价 | 元素和根的名称 | 元素和根的符号 | 常见的化合价 |
| 钾 | K | +1 | 氯 | Cl | -1、+1、+5、+7 |
| 钠 | Na | +1 | 溴 | Br | -1 |
| 银 | Ag | +1 | 氧 | O | -2 |
| 钙 | Ca | +2 | 硫 | S | -2、+4、+6 |
| 镁 | Mg | +2 | 碳 | C | +2、+4 |
| 钡 | Ba | +2 | 硅 | Si | +4 |
| 铜 | Cu | +1、+2 | 氮 | N | -3、+2、+3、+4、+5 |
| 铁 | Fe | +2、+3 | 磷 | P | -3、+3、+5 |
| 铝 | Al | +3 | 氢氧根 | OH- | -1 |
| 锰 | Mn | +2、+4、+6、+7 | 硝酸根 | NO3- | -1 |
| 锌 | Zn | +2 | 硫酸根 | SO42- | -2 |
| 氢 | H | +1 | 碳酸根 | CO32- | -2 |
| 氟 | F | -1 | 铵根 | NH4+ | +1 |
记忆口诀:
常见元素的化合价口诀
(1)一价钾、钠、银、氢、氟,二价钙、镁、钡和锌,铝价正三氧负二,以上价态要记真。铜一二来铁二三,碳硅二四要记全,硫显负二正四六,负三正五氮和磷,氯价最常显负一,还有正价一五七,锰显正价二四六,最高价数也是七。
(2)常见原子团的化合价口诀
一价铵根氢氧根,另有硝酸氯酸根。二价硫酸碳酸根,勿忘一个锰酸根。三价只有磷酸根。除了铵根皆为负,常写常用能记住。
相关初中化学知识点:元素的推断
元素推断题:
元素推断题是中学化学练习中的一种重要题型,该类题型以原子结构、周期表等为题干,集基本概念、基础理论及元素化合物知识于一身,具有综合性比较强的特点。
元素推断的规律:
一、原子结构与元素在周期表中的位置关系的规律
1.周期数=核外电子层数
2.族序数=主族元素的最外层电子数
3.质子数=原子序数=原子的核外电子数
4.主族元素的最高正价=族序数
5.最低负价=最高正价-8
二、根据族序数与周期序数的比值判断金属性与非金属性的强弱(族序数―m;周期―n)
1.
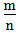 <1时,为金属,
<1时,为金属,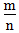 越小,金属性越强
越小,金属性越强2.
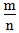 >1时,为非金属,
>1时,为非金属,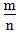 越大,非金属性越强
越大,非金属性越强 3.
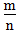 =1时,为两性元素
=1时,为两性元素 三、根据元素的性质,存在及用途的特殊性来推断元素
1.形成化合物种类最多的元素或单质是自然界中硬度最大的物质的元素,或气态氢化物中氢的质量分数最大的元素:C
2.空气中含量最多的元素或气态氢化物的水溶液呈碱性的元素:N
3.地壳中含量最多的元素,或气态氢化物沸点最高的元素,或氢化物在通常情况下呈液态的元素:O
4.地壳中含量最多的金属元素:Al
5.最活泼的非金属元素,或无正价的元素,或无含氧酸的非金属元素,或无氧酸可腐蚀玻璃的元素,或气态氢化物最稳定的元素,或阴离子的还原性最弱的元素:F
6.最活泼的金属元素,或最高正价氧化物对应的水化物碱性最强的元素,或阳离子氧化性最弱的元素:Cs
7.最容易着火的非金属元素的单质,其元素是:P
8.焰色反应:黄色:Na;紫色:K
9.最轻的单质的元素:H;最轻的金属元素:Li
10.常温下单质呈液态的非金属元素:Br;金属元素:Hg
11.两性元素:Al,Be,Zn
12.元素的气态氢化物和它的最高价氧化物对应的水化物起化合反应的元素:N
13.元素的气态氢化物能和它的氧化物在常温下反应,生成改元素的单质元素:S 14.常见的能形成同素异形体的元素:C,P,O,S
四、周期表中特殊位置的元素
1.族序数=周期数的元素:H,Be,Al
2.族序数=周期数2倍的元素:C
3.族序数=周期数3倍的元素:O
4.周期数是族序数2倍的元素:Li
5.周期数是族序数3倍的饿元素:Na
6.最高正价与最低负价代数和为零的短周期元素:C,Si
7.最高正价是最低负价绝对值3倍的短周期元素:S
8.除H外,原子半径最小的元素:F
9.短周期中离子半径最大的元素:S
10.最高正化合价不等于族序数的元素:F,O 五、元素周期表中的规律
五、元素周期表中的规律
1.各周期的元素种数(n表示周期序数)
(1)n为奇数:
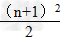
(2)n为偶数:
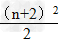
2.元素位置的确定
(1)根据原子结构示意图
①电子层数=周期序数
②最外层电子数=主族序数
(2)根据相近的稀有气体元素的原子序数:未知元素的原子序数-与之最接近的稀有气体元素的原子序数
①得数为正:该稀有气体的下一周期
②得数为负:与该稀有气体在同一周期
3.IIA族与IIIA族原子序数差值规律
(1)不跨过渡+1
(2)跨过过渡+11
(3)跨过锕镧+25
4.同主族元素的原子序数差值规律:左上右下规律
(1)IA族和IIA族(左):b=a+m
(2)IIIA族~VIIA族(右):b=a+n
(a:上一周期元素的原子序数;b:下一周期元素的原子序数;m:上一周期的元素种数;n:下一周期的元素种数)
5.阴上阳下规律:
(1)原子序数相同的阴阳离子,阴离子在上一周期,阳离子在下一周期
(2)离子半径:阴离子>阳离子
(3)原子半径:阴离子对应原子<阳离子对应原子
相关初中化学知识点:酸碱指示剂
酸碱指示剂:
跟酸或碱的溶液起作用而显示不同颜色的物质,叫酸碱指示剂,通常也简称指示剂。
紫色石蕊试液和无色酚酞试液的显色:
紫色石蕊试液和无色酚酞试液是两种常用的酸碱指示剂,它们与酸性、碱性溶液作用时显示的颜色见下表:
| 酸性溶液 | 碱性溶液 | 中性溶液 | |
| 石蕊试液 | 红 | 蓝 | 紫 |
| 酚酞试液 | 无 | 红 | 无 |
易错点:
①变色的是指示剂,而不是酸或碱的溶液。如盐酸使紫色石蕊试液变红,不能说成紫色石蕊试液使盐酸变红,但可以说紫色石蕊试液遇盐酸变红。
②酸或碱的溶液能使紫色石蕊试液或酚酞试液变色,但能使紫色石蕊试液或酚酞试液变色的不一定是酸或碱的溶液,还可能是酸性盐溶掖或碱性盐溶液。如碳酸钠溶液能使紫色石蕊试液变蓝,但碳酸钠不是碱,而是盐。
酸碱指示剂的代用品:
在自然界里,有许多植物色素在不同的酸碱性溶液中.都会发生特定的颜色变化。这些植物色素可以用作石蕊和酚酞等指示剂的代用品。一些植物的色素及其在酸碱性溶液中的颜色变化如下:
| 代用指示剂的颜色 | |||
| 在酸性溶液中 | 在中性溶液中 | 在碱性溶液中 | |
| 牵牛花 | 红色 | 紫色 | 蓝色 |
| 苏木 | 黄色 | 红棕色 | 玫瑰红色 |
| 紫萝卜皮 | 红色 | 紫色 | 黄绿色 |
| 月季花 | 浅红色 | 红色 | 黄色 |
| 美人蕉 | 淡红色 | 红色 | 绿色 |
版权声明:本文内容由互联网用户自发贡献,该文观点仅代表作者本人。本站仅提供信息存储空间服务,不拥有所有权,不承担相关法律责任。如发现本站有涉嫌抄袭侵权/违法违规的内容,请发送邮件至 lxy@jiyifa.cn 举报,一经查实,本站将立刻删除。