高中化学知识点:氨水
逍遥右脑 2015-11-28 08:42
氨水:
(1) 浓氨水:易挥发,密度小于水,浓度越大,密度越小,无色,有刺激性气味的液体,熔沸点较低,能导电
(2)氨水是混合物(液氨是纯净物),其中含有3种分子(NH3、NH3・H2O、H2O)和3种离子(NH4+和OH-、极少量的H+)。
氨水的性质:
①刺激性:因水溶液中存在着游离的氨分子。
②挥发性:氨水中的氨易挥发。
③不稳定性:―水合氨不稳定,见光受热易分解而生成氨和水。
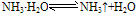
④弱碱性:氨水中一水合氨能电离出OH-,所以氨水显弱碱性,具有碱的通性:
A. 能使无色酚酞试液变红色,能使紫色石蕊试液变蓝色,能使湿润红色石蕊试纸变蓝。实验室中常见此法检验NH3的存在。
B. 能与酸反应,生成铵盐。浓氨水与挥发性酸(如浓盐酸和浓硝酸)相遇会产生白烟。
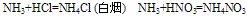
而遇不挥发性酸(如硫酸、磷酸)无此现象。实验室中可用此法检验NH3或氨水的存在。
工业上,利用氨水的弱碱性来吸收硫酸工业尾气,防止污染环境。
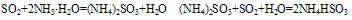
C. 沉淀性:氨水是很好的沉淀剂,它能与多种金属离子反应,生成难溶性弱碱或两性氢氧化物。例如:
生成的Al(OH)3沉淀不溶于过量氨水。
生成的白色沉淀易被氧化生成红褐色沉淀
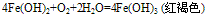
利用此性质,实验中可制取Al(OH)3、Fe(OH)3等。
D. 络合性:氨水与Ag+、Cu2+、Zn2+三种离子能发生络合反应,当氨水少量时,产生不溶性弱碱或两性氢氧化物,当氨水过量时,不溶性物质又转化成络离子而溶解。
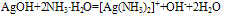
实验室中用此反应配制银氨溶液。
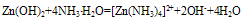
可用此反应来鉴别两性氢氧化物氢氧化铝和氢氧化锌。
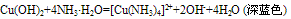
现出弱的还原性,可被强氧化剂氧化。如氨水可与Cl2发生反应:
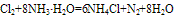
(4)氨水的保存方法:氨水对许多金属有腐蚀作用,所以不能用金属容器盛装氨水.通常把氨水盛装在玻璃容器、橡皮袋、陶瓷坛或内涂沥青的铁桶里。
氨水,液氨和一水合氨的比较:
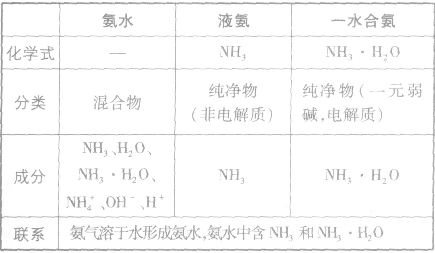
相关高中化学知识点:氯气
氯气:
①化学式:Cl2
②氯元素在周期表中的位置:第三周期ⅦA族
③氯原子的电子式: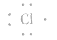
④氯的原子结构示意图: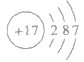
⑤氯原子的外围电子排布式: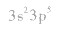
⑥化学键类型:非极性共价键
⑦氯分子的电子式: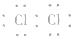
⑧氯分子的结构式: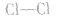
氯气的物理性质和化学性质:
(1)物理性质:黄绿色,有刺激性气味,有毒,密度比空气大,能溶于水(1:2)。
(2)化学性质:氯气(Cl2)是双原子分子,原子的最外层有七个电子,是典型的非金属元素,单质是强氧化剂。
①氯气与金属反应: 2Na+Cl2
 2NaCl(反应剧烈,产生大量白烟) 2Fe+3Cl2
2NaCl(反应剧烈,产生大量白烟) 2Fe+3Cl2 2FeCl3(反应剧烈,产生大量棕褐色烟,溶于水成黄色溶液) Cu+Cl2
2FeCl3(反应剧烈,产生大量棕褐色烟,溶于水成黄色溶液) Cu+Cl2 CuCl2(反应剧烈,产生大量棕色的烟,溶于水成蓝色或绿色溶液)氯气能与绝大数金属都能发生反应,表明氯气是一种活泼的非金属单质。
CuCl2(反应剧烈,产生大量棕色的烟,溶于水成蓝色或绿色溶液)氯气能与绝大数金属都能发生反应,表明氯气是一种活泼的非金属单质。 ②与非金属的反应 H2+Cl2
 2HCl(纯净的氢气在氯气中安静的燃烧,芒白色火焰,在瓶口处有白雾产生)H2+Cl2
2HCl(纯净的氢气在氯气中安静的燃烧,芒白色火焰,在瓶口处有白雾产生)H2+Cl2 2HCl(发生爆炸) 2P+3Cl2
2HCl(发生爆炸) 2P+3Cl2 2PCl3(液态) PCl3+Cl2==PCl5(固态)磷在氯气中剧烈燃烧,产生大量的烟、雾。雾是PCl3,烟是PCl5。氯气能有很多非金属单质反应,如S、C、Si等。
2PCl3(液态) PCl3+Cl2==PCl5(固态)磷在氯气中剧烈燃烧,产生大量的烟、雾。雾是PCl3,烟是PCl5。氯气能有很多非金属单质反应,如S、C、Si等。 ③与碱反应 Cl2+2NaOH==NaCl+NaClO+H2O 2Cl2+2Ca(OH)2==CaCl2+Ca(ClO)2+2H2O
④与某些还原性物质反应:Cl2+2FeCl2===2FeCl3 Cl2+SO2+2H2O==2HCl+H2SO4
⑤有机反应(参与有机反应的取代和加成反应)
CH4+Cl2→CH3Cl+HCl
CH3Cl+Cl2→CH2Cl2+HCl
CH2Cl2+Cl2→CHCl3+HCl
CHCl3+Cl2→CCl4+HCl
Cl2+CH2=CH2→CH2Cl-CH2Cl(加成反应)
⑥与水反应 Cl2+H2O
 HCl+HClO
HCl+HClO 版权声明:本文内容由互联网用户自发贡献,该文观点仅代表作者本人。本站仅提供信息存储空间服务,不拥有所有权,不承担相关法律责任。如发现本站有涉嫌抄袭侵权/违法违规的内容,请发送邮件至 lxy@jiyifa.cn 举报,一经查实,本站将立刻删除。